COVID-ассоциированный инвазивный легочный аспергиллез: проблемы диагностики и лечения

Фото носит иллюстративный характер. Из открытых источников.
Инвазивный легочный аспергиллез (ИЛА) является серьезным осложнением респираторных вирусных инфекций, протекающих в тяжелой форме, особенно у пациентов в отделениях реанимации. Крупная когорта таких больных была зарегистрирована в течение сезонов гриппа H1N1 2009–2011 годов. В период пандемии COVID-19 проблема приобрела еще большую актуальность. Коронавирусная пневмония, осложненная присоединением грибковой микрофлоры рода Aspergillus, резко ухудшает прогноз, увеличивает продолжительность лечения и число неблагоприятных исходов. При отсутствии специфической терапии летальность от СОVID-ассоциированного инвазивного легочного аспергиллеза составляет 100 %.
О сложностях диагностики и особенностях лечения COVID-ИЛА рассказала Наталья Матиевская, заведующая кафедрой инфекционных болезней ГрГМУ, доктор мед. наук, профессор.
Возбудитель — грибы рода Aspergillus

Наталья Матиевская:
Из более 100 известных науке видов плесневых грибов рода Aspergillus около 20 являются потенциальными возбудителями аспергиллеза у человека. В 90 % случаев это Aspergillus fumigatus, примерно 8–9 % A. flavus, менее 2 % A. niger и в очень редких случаях A. nidulans. С тяжелым торпидным течением бронхолегочного аспергиллеза связывают A. niger.
Аспергиллы хорошо видны под микроскопом, имеют специфическую морфологическую картину, которая позволяет их легко верифицировать. В мазках из патологического материала обнаруживаются бесцветные, септированные гифы мицелия. Это строгие аэробы, на среде Сабуро при температуре 20–25 °C растут в виде пушистых колоний, которые быстро меняют цвет.
Ниша обитания аспергилл весьма обширна, они распространены по всему миру, существуют в разных климатических условиях в почве, воде, воздухе, на деревьях, растениях, в перьях птиц и шерсти животных. В быту — на овощах, фруктах, продуктах питания, на стенах помещений в виде черной плесени.
Влажные, плохо проветриваемые помещения обсеменены спорами аспергилл. В организм человека возбудитель попадает аэрогенным путем, при вдыхании частиц пыли со спорами, реже — контактным путем через микротравмы на коже. В большинстве случаев входными воротами инфекции служат легкие и придаточные пазухи носа.
Любой человек ежедневно вдыхает споры плесневых грибов, однако у подавляющего большинства людей это не приводит к развитию инвазивных заболеваний. Риск значительно возрастает при иммуносупрессии. При этом далеко не у каждого пациента даже с тяжелым течением гриппа или коронавирусной инфекции развивается инвазивный легочный аспергиллез.
Наталья Матиевская:
Еще в период эпидемий гриппа 2009–2011 годов было замечено, что при тяжелом течении присоединение плесневой микрофлоры происходит, как правило, у пациентов именно в реанимации, особенно находящихся на ИВЛ. В среднем в 19 % случаев, то есть у каждого пятого.
То же самое отмечается и в период пандемии COVID-19. По разным данным, ассоциированный с COVID-19 инвазивный аспергиллез легких в среднем встречается у 2,5–15 % пациентов с коронавирусной инфекцией. Среди пациентов на ИВЛ — у 18–35 %.
Факторы риска возникновения COVID-ИЛА:
Специалист обратила внимание, что среди факторов риска, на которые повлиять невозможно (наличие коморбидной патологии, избыточная масса тела и пр.), есть ряд ятрогенных факторов, связанных с аспектами лечения тяжелых пневмоний. Поэтому всегда нужно анализировать назначаемое лечение, особенно это касается массированной, неоправданной антибиотикотерапии.
Диагностические Критерии COVID-ИЛА
Основным клиническим вариантом COVID-ИЛА является пневмония. Реже встречается язвенный трахеобронхит. Без специфического лечения происходит гематогенная диссеминация с поражением ЦНС и других органов.
Наталья Матиевская:
Как правило, COVID-ИЛА развивается на 3–9-е сутки после поступления пациента в ОРИТ или 3–6-е сутки после подключения его к ИВЛ, эти сроки могут варьировать от 2 до 35 дней. Международные критерии диагностики COVID-ИЛА были опубликованы в 2020 году Европейской конфедерацией медицинской микологии (ECMM), Международным обществом медицинской и ветеринарной микологии (ISHAM).
Мы широко ими пользуемся. В последней 15-й версии российских временных методических рекомендаций «Профилактика, диагностика и лечение новой коронавирусной инфекции COVID-19» также представлены диагностические критерии и подходы к современной терапии COVID-ИЛА.
Клинические признаки COVID-ИЛА (неспецифические)
У пациента с верифицированной инфекцией COVID-19, тяжелым течением, ОРДС при появлении любого из следующих признаков:
Радиологические признаки COVID-ИЛА
Отрицательная динамика результатов рентгенограммы или КТ органов грудной клетки в виде появления новых очагов инфильтрации или деструкции ткани легкого, прогрессирования признаков вирусного поражения легких. К типичным радиологическим признакам ИЛА относят узлы, полости, halo, наличие сегментарной или долевой консолидации.
«Радиологические признаки синусита также должны вызывать настороженность в плане риска инвазивных микозов. В комплексе с другими клиническими и радиологическими признаками наличие поражения придаточных пазух носа ассоциируется с подозрением на грибковую инфекцию».
Инвазивный аспергиллезный трахеобронхит, который встречается гораздо реже, имеет характерные проявления при бронхоскопии: трахеобронхиальные изъязвления, узелки, псевдомембраны, налеты или струп на слизистой бронхов. Диагностика дополняется микроскопическими и микологическими лабораторными тестами.
Подтвержденный, вероятный и возможный случаи COVID-ИЛА
Диагностика ИЛА у пациентов в ОРИТ далеко не всегда оказывается успешной. По данным мировой статистики результатов аутопсий, 53–60 % случаев ИЛА в ОРИТ не диагностируется при жизни. Поэтому еще в начале 2000-х годов международными экспертами было предложено классифицировать ИЛА в зависимости от наличия диагностических критериев и лабораторного подтверждения: доказанный, вероятный и возможный. Это сделано для того, чтобы своевременно начать таргетное лечение.
Наталья Матиевская:
Важно понимать, что каждый из случаев является показанием для проведения специфического лечения в полном объеме.
Подтвержденный случай COVID-ИЛА: у пациента с наличием клинических и радиологических критериев диагностики этиология аспергиллеза доказана микробиологическим исследованием материала, взятого путем стерильной аспирации или биопсии участка поврежденного легкого, полученного при фибробронхоскопии.
Микробиологическое исследование материала проводится двумя стандартными базовыми методами идентификации возбудителя: микроскопия материала с окраской образцов калькофлюором белым (грибковые элементы Aspergillus демонстрируют инвазивный рост с повреждением окружающих тканей) и выделение культуры Aspergillus и/или ДНК аспергилл.
Вероятный случай COVID-ИЛА: верификация этиологии аспергиллеза на основании исследования бронхоальвеолярного лаважа (БАЛ) и положительного результата галактоманнанового (ГМ) теста с учетом результатов лучевой диагностики и клинических данных.
Микробиологические тесты: обнаружение элементов аспергилл при микроскопии БАЛ; или выделение культуры аспергилл из БАЛ (посев на среду Сабуро) либо ДНК аспергилл методом ПЦР; или положительный ГМ-тест с ИОП ≥ 1,0 при исследовании БАЛ либо ИОП > 0,5 при исследовании сыворотки крови или комбинация данных тестов.
Наталья Матиевская:
Галактоманнан является основным компонентом клеточной стенки аспергилл и при инвазивных формах обнаруживается в крови. Он очень информативен как при выявлении в сыворотке крови, так и в БАЛ.
Возможный случай COVID-ИЛА: базируется на комбинации микробиологических исследований небронхоальвеолярного лаважа (НБЛ) или трахеального аспирата (ТА) у интубированных пациентов, с учетом радиологических и клинических данных.
Микробиологические тесты: обнаружение элементов аспергилл при микроскопии (НБЛ/ТА) или выделение культуры из НБЛ/ТА и/или ДНК аспергилл методом ПЦР; или положительный ГМ-тест с ИОП ≥ 1,0 при исследовании НБЛ/ТА при повторном определении; или положительный ГМ-тест с ИОП > 0,5 при исследовании сыворотки крови или комбинация данных тестов.
Наталья Матиевская:
При возможном случае COVID-ИЛА мы не имеем достаточно убедительных критериев верификации, потому что используем НБАЛ, ТА, иногда даже мокроту. Но этот случай выделен экспертами для того, чтобы клиницисты могли и должны (!) начинать адекватную противогрибковую терапию аспергиллеза. Такие случаи не рекомендуется включать в клинические исследования.
Культура аспергилл из БАЛ или НБЛ: подводные камни
Наиболее достоверные результаты при подтверждении ИЛА получаются при исследовании биоптата легочной ткани, полученного при фиброгастроскопии. Однако в реальной клинической практике взять такой биоматериал весьма непросто, если речь идет о тяжелых пациентах в реанимации. Это несет высокие риски для пациента.
Наталья Матиевская:
Никто из реаниматологов не рискнет проводить прижизненную биопсию ткани легкого у критического пациента с COVID-19. Использование же в качестве биоматериала БАЛ или НБЛ не позволяет достоверно различить ИЛА и колонизацию дыхательных путей аспергиллами, которая часто встречается у пациентов с сопутствующей хронической патологией органов дыхания, например, ХОБЛ, у курильщиков. Поэтому к постановке диагноза ИЛА у таких пациентов нужно подходить комплексно.
Наличие галактоманнана в БАЛ также не позволяет дифференцировать ИЛА и колонизацию аспергиллами дыхательных путей.
Наталья Матиевская:
Гораздо более надежный тест для ИЛА — наличие галактоманнана в сыворотке крови. Это высокоспецифичный тест, и если он положительный, то это точно аспергиллез. Однако чувствительность при COVID-ИЛА не превышает 20 %. Это означает, что у 80 % пациентов ложноотрицательные результаты и, к сожалению, они могут оставаться недиагностированными. Также следует помнить, что ГМ-тест может давать ложноположительные результаты у пациентов, принимавших пиперациллин + тазобактам и коамоксиклав.
Дополнительные лабораторные тесты. Определение 1,3-beta-delta-glucan может повышать информативность диагностики ИЛА до 90 %, но не является специфичным тестом для аспергиллеза. Определение ДНК аспергилл методом ПЦР в биоматериале (биоптаты легкого, БАЛ, НБЛ) было включено в международные рекомендации по выявлению ИЛА в 2020 году, необходимо получить 2 положительных результата ПЦР для подтверждения диагноза.
Примеры из практики

Рисунок 1. Смешанная вирусно- бактериальная пневмония, осложненная аспергиллезом.
Справа хорошо видны аспергиллы, слева — инфильтрация нейтрофилами, кровоизлияния в альвеолы.
Желтые стрелки — гнойный экссудат, синие — кровоизлияния, зеленые — гифы аспергилл среди экссудата, красная стрелка — гиалиновая мембрана.
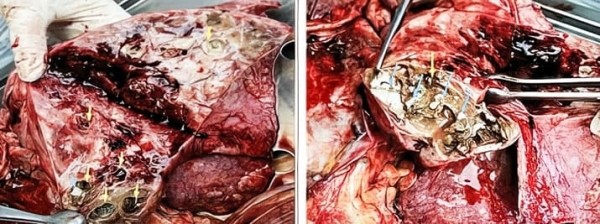
Рисунок 2. Двусторонняя сливная абсцедирующая бактериально-грибковая пневмония (аспергиллез), правостороний гнойный плеврит (1000 мл, грам+ кокки St. аureus, Аctinobacter baumannii).
На разрезе легкого видны множественные абсцессы различных размеров (желтые стрелки), колонии аспергилл (синие стрелки).

Рисунок 3. Колония аспергилл среди тканевого детрита и гнойного экссудата.
Лечение COVID-ИЛА
Возбудители COVID-ИЛА чувствительны in vitro к вориконазолу, изавуконазолу, каспофунгину, амфотерицину В.
«Аспергиллы устойчивы к флуконазолу! При наличии рисков ИЛА прием пациентом флуконазола не должен успокаивать врача и убеждать в том, что он получает адекватную противогрибковую терапию».
Препараты первой линии выбора при терапии подтвержденного, вероятного или возможного случая COVID-ИЛА: вориконазол или изавуконазол — противогрибковые препараты широкого спектра действия из группы триазолов.
Наталья Матиевская:
Вориконазол имеет высокий риск межлекарственного взаимодействия, так как метаболизируется через систему изоферментов CYP2C19, CYP2C9, CYP3A4. В сравнении с ним изавуконазол обладает меньшей токсичностью и менее выраженным лекарственным взаимодействием. Липосомальный амфотерицин В нефротоксичен, что необходимо учитывать у тяжелых пациентов с COVID-19, т. е. у многих из них имеется острая почечная недостаточность.
Препараты второй линии: позаконазол — противогрибковое средство для системного применения из группы производных триазола или эхинокандины (анидулафунгин, каспофунгин, микафунгин).
Наталья Матиевская:
Эхинокандины не должны использоваться как монотерапия для лечения ИЛА, они рекомендуются в комбинации с вориконазолом или изавуконазолом при наличии резистентности к азолам и должны рассматриваться как терапия спасения у крайне тяжелых пациентов.
Продолжительность противогрибковой терапии COVID-ИЛА в настоящее время не установлена, оптимальным считается лечение в течение 6–12 недель.
Клинический случай
Пациент К., 49 лет. Заболел, когда находился за границей в служебной командировке. Госпитализирован с COVID-19, подтвержденным ПРЦ-тестом, внегоспитальной двусторонней полисегментарной пневмонией, дыхательной недостаточностью 1-й ст. В течение 2 недель проходил лечение без особых улучшений. На 19-е сутки вернулся в Беларусь, был госпитализирован в стационар, перепрофилированный для лечения COVID-19.
На момент поступления состояние среднетяжелое. Жалобы на одышку, кашель с мокротой, слабость, потливость. Температура до 39 °C, сатурация до 90 %. Тахикардия, в легких мелкопузырчатые влажные звучные хрипы с обеих сторон, больше справа в проекции верхней доли.
Диагноз при поступлении: коронавирусная инфекция, подтвержденная ПЦР, тяжелая форма; внегоспитальная двусторонняя полисегментарная вирусно-бактериальная пневмония, вероятно, с абсцедированием справа в верхней доле, тяжелое течение; дыхательная недостаточность 2-й ст.
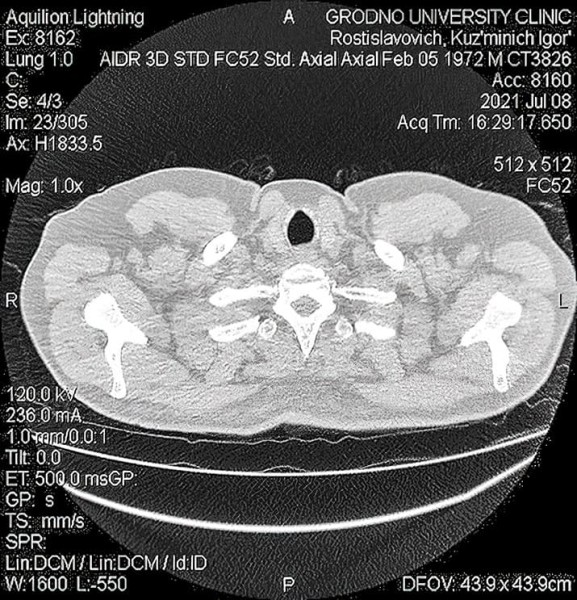
КТ органов грудной клетки: множественные консолидации в легких, отрицательная динамика в сравнении с предыдущими результатами. Воспалительные изменения по интерстициальному типу, которые с высокой степенью вероятности могут быть ассоциированы с вирусной пневмонией. Степень тяжести КТ-3.
Лечение: с антибактериальной целью имипенем в/в капельно, кислородотерапия 7 л/мин. Учитывая вероятность абсцедирования, от назначения глюкокортикостероидов воздержались. Пациенту назначены исследования на прокальцитонин и ГМ-тест.
Прокальцитонин: 0,08 (норма). ГМ-тест сыворотки крови положительный.
После получения этих результатов пациенту выставлен диагноз: аспергиллез легких. Сразу же отменяется антибиотик, в схему лечения включен вориконазол 300 мг внутривенно по схеме: 2 раза в первый день, далее по 200 мг 2 раза в день. Отмечается медленная положительная динамика.
Через 20 дней пациент выписан на амбулаторное наблюдение с улучшением. Рекомендовано продолжать прием вориконазола 200 мг 2 раза в день под контролем клинико-лабораторных и радиологических данных.
Иллюстрации предоставлены Н. Прокопчиком, доцентом кафедры патанатомии ГрГМУ.
Источник: medvestnik.by
Комментарии закрыты.