Природа хронической гастродуоденальной боли. Часть 1

Фото носит иллюстративный характер. Из открытых источников.
Природа хронической гастродуоденальной боли. Часть 1
Хроническая боль в животе — боль, которая присутствует на протяжении более 3 месяцев. Она может беспокоить постоянно или периодически (рецидивирующая). Может исходить из любой системы, включая мочеполовую, желудочно-кишечную и гинекологическую.
Этиология
У детей наиболее частые причины хронической абдоминальной боли — непереносимость лактозы, запор и гастроэзофагеальная рефлюксная болезнь. У молодых людей — диспепсия (пептическая язва или другие причины), реактивный гастрит (вызванный аспирином или НПВС, напитками наподобие колы и острой пищей), заболевания печени, в т. ч. желчнокаменная болезнь (холецистит) или гепатиты, заболевания поджелудочной железы (панкреатиты), паразитарная инфекция (лямблиоз), воспалительные заболевания кишечника (язвенный колит, болезнь Крона), синдром раздраженного кишечника. У лиц старшего возраста хроническая абдоминальная боль, как правило, связана с раком желудка, поджелудочной железы, толстой кишки или яичников.
На самом деле этиология так широка, что мы обсуждаем только наиболее частые заболевания верхнего отдела ЖКТ.
Боль в эпигастрии и верхней части живота может указывать на пищеводное (к примеру, гастроэзофагеальный рефлюкс), желудочное (гастриты), дуоденальное (язва), желчное (холецистит) или панкреатическое ее происхождение.
Также ключом к диагнозу можно назвать информацию о факторах усиления или ослабления боли. Спровоцированная приемом пищи, она иногда указывает на язву желудка, хронический панкреатит, желчнокаменную болезнь, абдоминальную ишемию (так называемая брюшная ангина) или функциональные расстройства, включая синдром раздраженного кишечника, функциональную диспепсию или постпрандиальный дистресс-синдром.
Боль, ослабевающая после приема пищи, предполагает пептическую язвенную болезнь 12-перстной кишки. Уменьшающаяся после дефекации может указывать на синдром раздраженного кишечника. Связанная с менструальным циклом говорит о гинекологическом происхождении. Боль, ассоциированная с частым мочеиспусканием, предполагает интерстициальный цистит.
Диагностика
В анамнезе врач должен учитывать сопутствующие симптомы, включающие лихорадку, ночное потение, тошноту или рвоту, диарею, запор, кровавый стул, изменения в характере стула, анемию, потерю/набор веса.
Физикальное исследование вначале должно быть направлено на витальные признаки. Лихорадка, тахикардия, тахипноэ и гипотензия предполагают острое заболевание, требующее срочной реакции. Осмотр головы и шеи позволяет выявить неспецифические признаки внутрибрюшной патологии, включающие «височное запустение», запавшие глаза, выступающие ключицы, что обусловлено значительным похудением. Сухость слизистых оболочек указывает на дегидратацию. Иктеричность склер позволяет заподозрить гепатобилиарное заболевание. Бледность конъюнктивы говорит об анемии. Заболевания периферических сосудов, проявляющиеся снижением пульса, могут сочетаться с брюшной ангиной или мезентериальной ишемией. Боль на вдохе предполагает отраженную боль из легких или боль в правом/левом верхнем квадранте.
Связь между хронической абдоминальной болью и посттравматическим стрессом, алкоголизмом, тревогой и депрессией хорошо изучена. Физические, психологические или эмоциональные воздействия в семье порой выступают важным триггером, особенно у детей и подростков. Изучение психосоциальных факторов призвано помочь в минимизации исследований.
Эмоциональные (аффективные) расстройства могут способствовать хронизации боли. Симптомы неустойчивого настроения и психического состояния должны быть тщательно исследованы.
Специфический алгоритм для диагностики хронической абдоминальной боли не разработан. Исходить следует из анамнеза и данных физикального исследования, а также на основе опыта; при отсутствии тревожных признаков прибегать к лабораторным тестам и методам визуализации, эффективным по затратам.
Стандартные лабораторные тесты: общий анализ крови для скрининга инфекции или анемии, количество тромбоцитов и показатели СОЭ (могут указывать на воспалительный процесс), электролиты сыворотки, глюкоза, креатинин и мочевина (для изучения метаболических процессов), функциональные печеночные тесты, липаза и амилаза (особенно у пациентов с болью в верхней части живота), анализ и посев мочи (помогает исключить инфекции мочевых путей и интерстициальный цистит).
Дополнительные лабораторные тесты (в индивидуальных случаях) включают анализ кала на цисты и паразиты (если подозревается лямблиоз), тест на беременность (должен быть выполнен
до рентгенологического и эндоскопического исследования), серологический анализ на Н. рylori (у пациентов с жалобами на проблемы верхнего отдела желудочно-кишечного тракта, включая раннюю насыщаемость и дискомфорт в эпигастрии, т. е. с симптомами диспепсии).
Все пациенты старше 50 лет с болью в животе должны быть подвергнуты эндоскопии. Колоноскопия показана, если имеется боль в нижней части живота и/или связь с нарушениями в характере стула. А ранняя верхняя эндоскопия — если боль локализована в верхней части живота, особенно при наличии других желудочно-кишечных симптомов (ранняя насыщаемость, тошнота, рвота). Нет рекомендаций, когда такие исследования должны быть проведены у молодых пациентов (младше 50 лет).
УЗИ живота показано для исследования боли, локализованной в правом верхнем квадранте или в эпигастрии, особенно если повышены уровни печеночных и панкреатических ферментов. УЗИ таза и трансвагинальное и/или трансректальное проводятся при боли в нижней части живота.
КТ может помочь в исследовании дилатированных петель кишечника, исключении частичной кишечной непроходимости, выявлении патологии в других органах (поджелудочной железе, печени, почках и др.), идентификации воспалительных процессов (к примеру, воспалительные заболевания толстой кишки, дивертикулиты, абсцессы), исследовании забрюшинного пространства или таза.
Классификация гастритов
Острые гастриты — термин, объединяющий широкий спектр раздражителей, вызывающих воспалительные изменения в слизистой желудка. Гастриты — очень туманное понятие, означающее различные проявления у разных людей. Пациенты и врачи часто относят к гастритам диспепсические симптомы, в то время как эндоскописты обнаруживают эндоскопические доказательства воспаления. С другой стороны, патологи полагаются на гистопатологические признаки. Корреляция их с эндоскопическими данными низкая.
При различной этиологии общие клинические проявления отличаются уникальными гистологическими характеристиками. Воспаление может затронуть весь желудок (пангастрит) или отдельную область (антральный гастрит).
Аденокарцинома желудка, как полагают, возникает в результате каскада, который был впервые описан французским патоморфологом Р. Correa в 1988 году и включает неатрофический и атрофический гастриты, кишечную метаплазию, дисплазию и, наконец, рак желудка (см. рис. 1). Механизм, лежащий в основе данного процесса, остается неясным, но предположительно связан с инфекцией H. pylori (De Luca A., Iaquinto G., 2004). Атрофический гастрит и кишечная метаплазия желудка повышают риск прогрессирования в рак желудка — эти состояния являются фоном, на котором развивается дисплазия и затем аденокарцинома.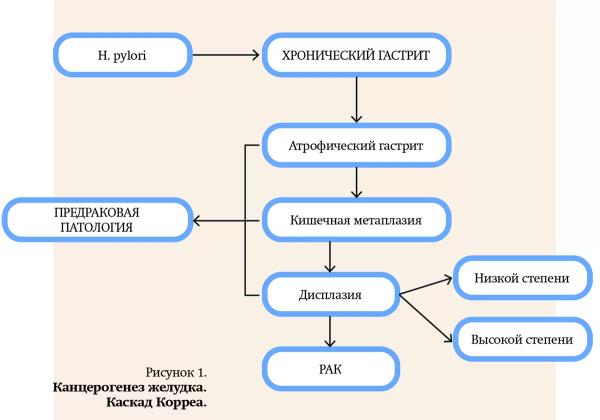
Острый гастрит может быть разделен на 2 категории: эрозивный (например, поверхностные, глубокие, геморрагические эрозии) и неэрозивный. Первый возникает в результате химического повреждения, вызванного алкоголем, НПВС, кортикостероидами и сильным физикальным стрессом, таким как травма головы, операция, сепсис, ожоги и гипотермия. Острый нейтрофильный гастрит ассоциируется с инфекцией Н. рylori.
Гастриты могут быть широко классифицированы на неатрофическую, атрофическую и специальные формы. Первые обычно связаны с Н. рylori, атрофические формы ассоциируются с Н. рylori и аутоиммунными заболеваниями, специальные включают химически-индуцированные или индуцированные радиацией, лимфоцитарные, гранулематозные, эозинофильные и инфекционные гастриты.
Гастрит — воспалительное состояние слизистой желудка, которое гистопатологически диагностируется воспалительно-клеточной инфильтрацией, состоящей в основном из мононуклеарных клеток, в том числе лимфоцитов и плазматических клеток. Фенотипическое различие между неатрофическим и атрофическим гастритами общепризнано. Последний определяется как потеря нормального железистого эпителия желудка и замена метапластической железистой структурой или фиброзом собственной пластинки (Dixon M. F. et al., 1996).
Повреждение клеток эпителия и регенерацию без воспаления вернее называть гастропатией. Она может быть диагностирована без гистологических доказательств и по внешнему виду при эндоскопии или радиологии. Гастропатии обычно вызваны раздражителями, в том числе лекарствами (например, НПВС) и алкоголем, рефлюксом желчи, гиповолемией и хроническим застоем.
Атрофический гастрит включает аутоиммунный метапластический атрофический гастрит и хеликобактерный метапластический атрофический гастрит (мультифокальный). Аутоиммунный локализован в теле и своде желудка. Он характеризуется тяжелой диффузной атрофией ацидофильных желез и ассоциируется с ахлоргидрией, антителами к внутреннему фактору, антителами к париетальным клеткам, гипергастринемией, анемией, связанной с дефицитом железа и мальабсорбцией витамина В12. Атрофический гастрит ассоциируется с повышенным риском злокачественности желудка. При мультифокальном атрофическом гастрите воспаление в антруме и теле желудка, как правило, происходит при инфекции Н. рylori.
После нескольких лет хронического гастрита слизистая оболочка желудка может стать атрофической (истонченной и просвечивающейся), легко визуализируются вены подслизистой оболочки. В тяжелых случаях складки, в норме присутствующие в верхней половине желудка, сглажены или отсутствуют (атрофия желудка). Секреция кислоты снижена или отсутствует. Такое состояние приводит к аденокарциноме желудка, анемии, дисбиозу. H. pylori и аутоиммунность — главные причины.
Однако в большинстве случаев перечисленные признаки отсутствуют. У детей их вовсе нет. Обычная эндоскопия в режиме белого света не может точно дифференцировать пренеопластические состояния желудка (Dinis-Ribeiro M. et al., 2012). Скрининг гипо- и ахлоргидрии позволяет диагностировать невидимый атрофический гастрит. Проводится измерение рН желудочного сока — по чувствительности оно равноценно электрической рН-метрии желудочным зондом.
При рН желудочного содержимого больше 6,0 применяют тест с рН-индикатором конго красным, орошая им тело желудка. При отсутствии изменения окраски на черную диагностируется анацидность. После этого проводится биопсия на морфологическую верификацию гастрита (антрум и тело желудка) и H. pylori. При положительном тесте на H. pylori выполняется эрадикация инфекции, что позволяет улучшить гистологическую картину атрофического гастрита и восстановить кислотность. При отрицательном подозревается аутоиммунный атрофический гастрит и проводится соответствующая диагностика (см. рис. 2).
Уровни пепсиногена сыворотки могут предсказать запущенный атрофический гастрит. Так, снижение уровня пепсиногена 1 (или соотношения пепсиногена 1/2) способствует определению повышенного риска атрофического гастрита и рака желудка. У пациентов с низким уровнем пепсиногена сыворотки обнаружение H. pylori может быть успешным для дальнейшего выявления лиц высокого риска (Dinis-Ribeiro M. et al., 2012).
Патологические состояния, ассоциированные с гипо- и ахлоргидрией
У пациентов с кишечной метаплазией эрадикация H. pylori не вызывает обратимость кишечной метаплазии, но может замедлить прогрессирование в неоплазию (Dinis-Ribeiro M. et al., 2012). В настоящее время применение ингибиторов ЦОГ-2 для уменьшения риска прогрессии предраковой патологии в аденокарциному желудка не поддерживается. Использование пищевых добавок с антиоксидантами как лечение для уменьшения частоты атрофии или кишечной метаплазии не подтверждается (Dinis-Ribeiro M. et al., 2012).
(Продолжение материала здесь.)
Источник: medvestnik.by
Комментарии закрыты.